蛋白标记定量服务
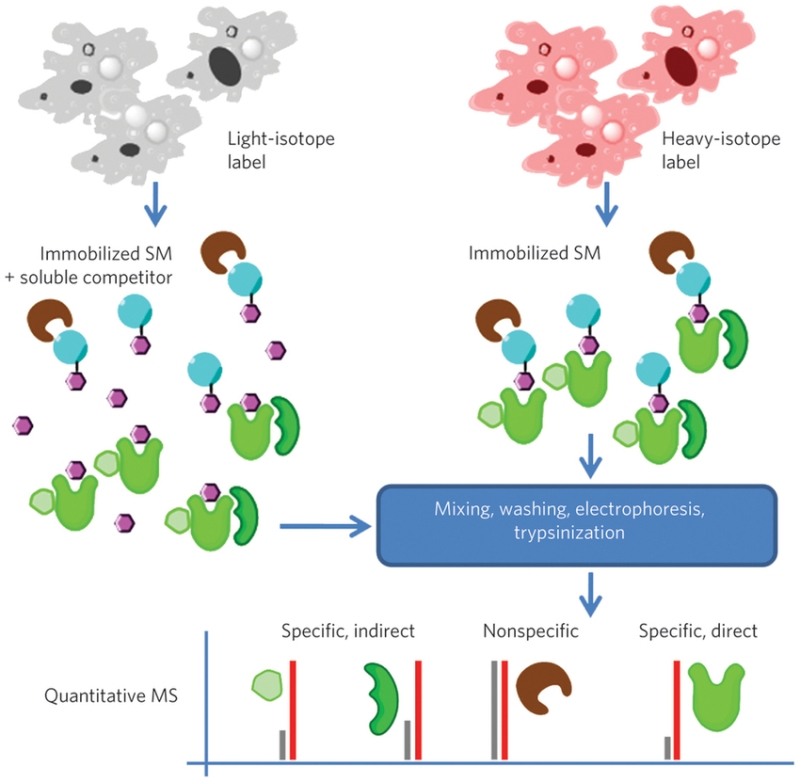
蛋白标记定量服务通过对标记类型、标记位点及标记比例的精确控制,实现蛋白信号的可量化与高度一致性,广泛应用于分子互作分析、定量检测及功能研究。我们依托成熟的标记与定量技术平台,为不同类型蛋白提供稳定、可重复的标记解决方案。
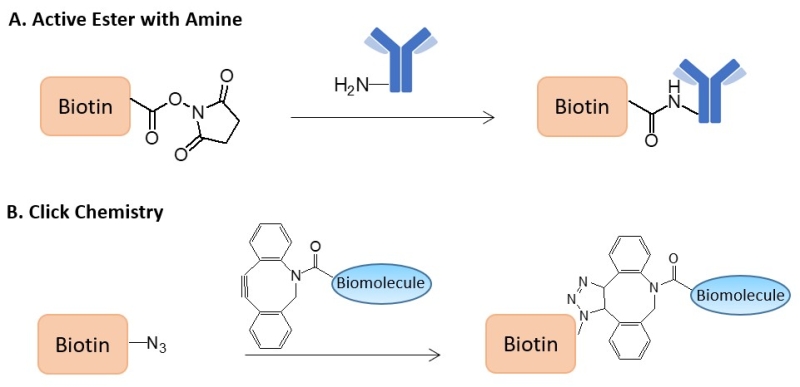
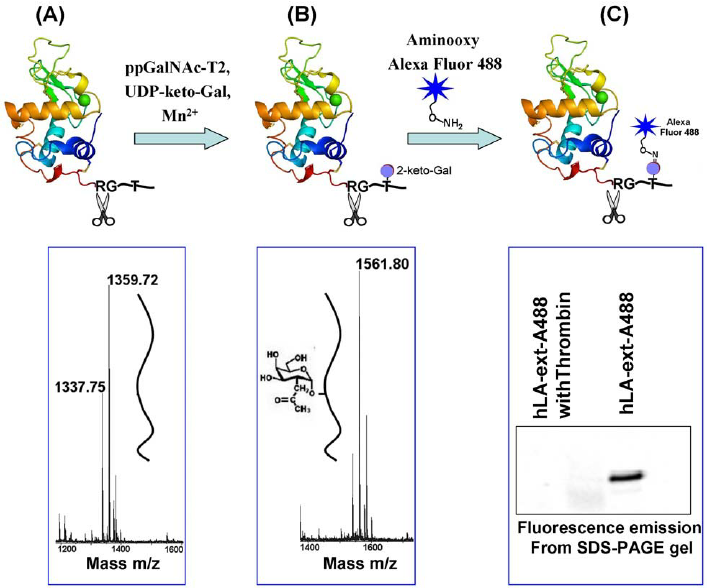
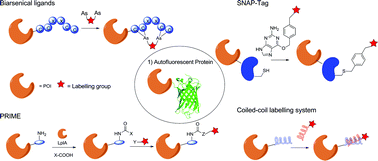
服务过程中根据蛋白结构特征与下游实验需求,合理选择荧光、生物素或化学标记方式,并对标记比例进行严格优化与验证,确保不影响蛋白构象与生物学活性。交付产品经过系统质量检测,可直接适配 SPR、BLI、MST 等多种检测平台,为科研与药物研发提供可靠的数据支持。