关键信息
-
基因名
Fractalkine/CX3CL1
- 应用
-
别名
NTN; ABCD3; C3Xkine; CXC3; CXC3C; NTT; SCYD1; ABCD3; FKN; Neurotactin; Fractalkine; Small Inducible Cytokine Subfamily D(Cys-X3-Cys)Member 1
-
种属
Mouse
-
表达系统
E. coli
-
标签
N-His
-
纯度
Greater than 97% as determined by SDS-PAGE.
-
蛋白编号
O35188
-
表达区间
Gln83~Pro330
-
蛋白长度
Partial
-
分子量
27kDa
-
内毒素
< 1.0 EU per μg protein as determined by the LAL method.
-
性状
Freeze-dried powder
-
缓冲液
PBS, pH7.4, containing 0.01% SKL, 1mM DTT, 5% Trehalose and Proclin300.
-
复溶方法
Reconstitute in ddH2O to a concentration of 0.1-0.5 mg/mL. Do not vortex.
- 个性化定制
-
稳定性测试
The thermal stability is described by the loss rate. The loss rate was determined by accelerated thermal degradation test, that is, incubate the protein at 37℃ for 48h, and no obvious degradation and precipitation were observed. The loss rate isless than 8% within the expiration date under appropriate storage condition.
-
保存条件 & 期限
Samples are stable for up to twelve months from date of receipt at -20℃ to -80℃. Store it under sterile conditions at -20℃ to -80℃. It is recommended that the protein be aliquoted for optimal storage. Avoid repeated freeze-thaw cycles.
-
运输条件
In general, recombinant proteins are supplied as lyophilized powder and shipped at ambient temperature. For bulk packages, the proteins are provided as frozen liquid and shipped with blue ice, unless otherwise requested by the customer.
质检流程
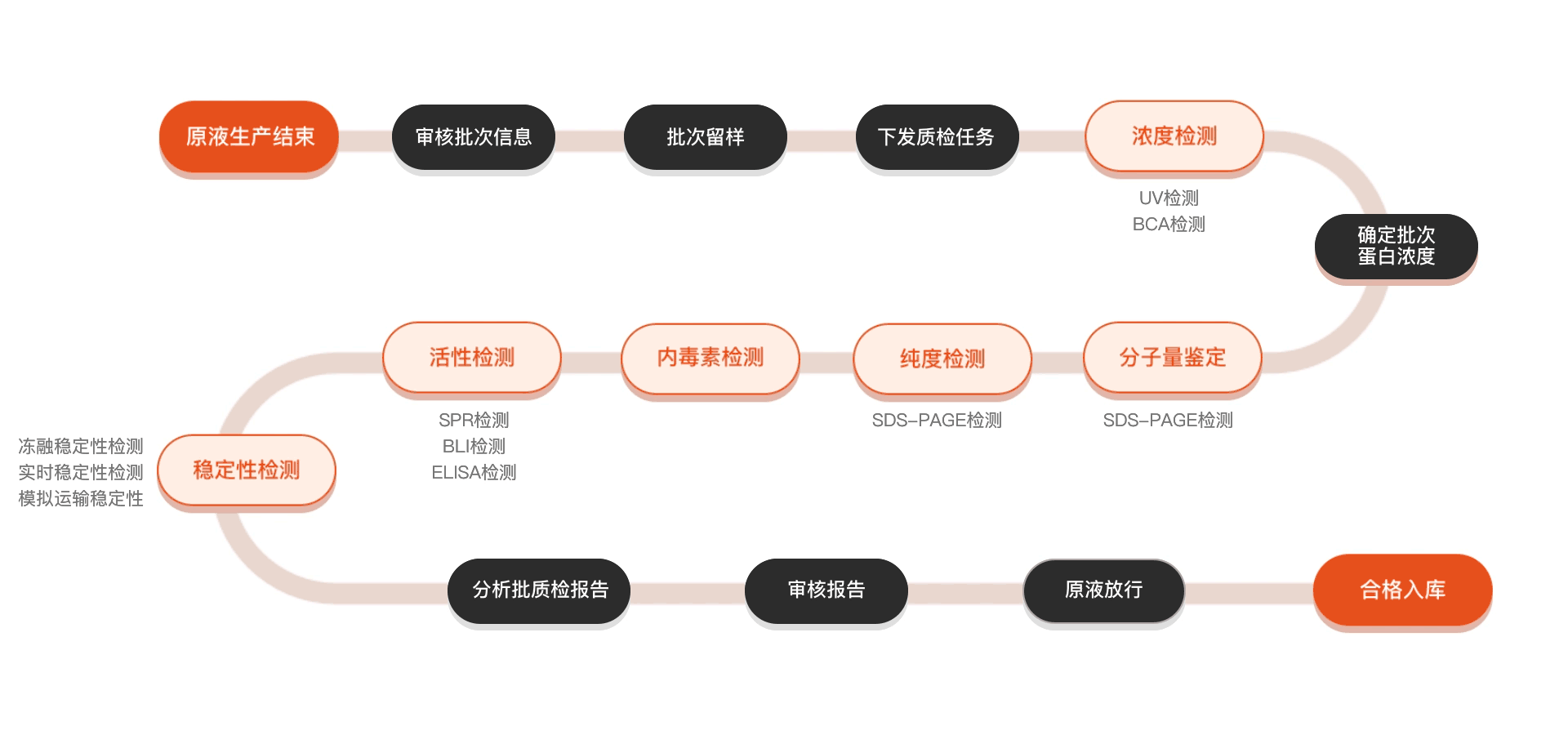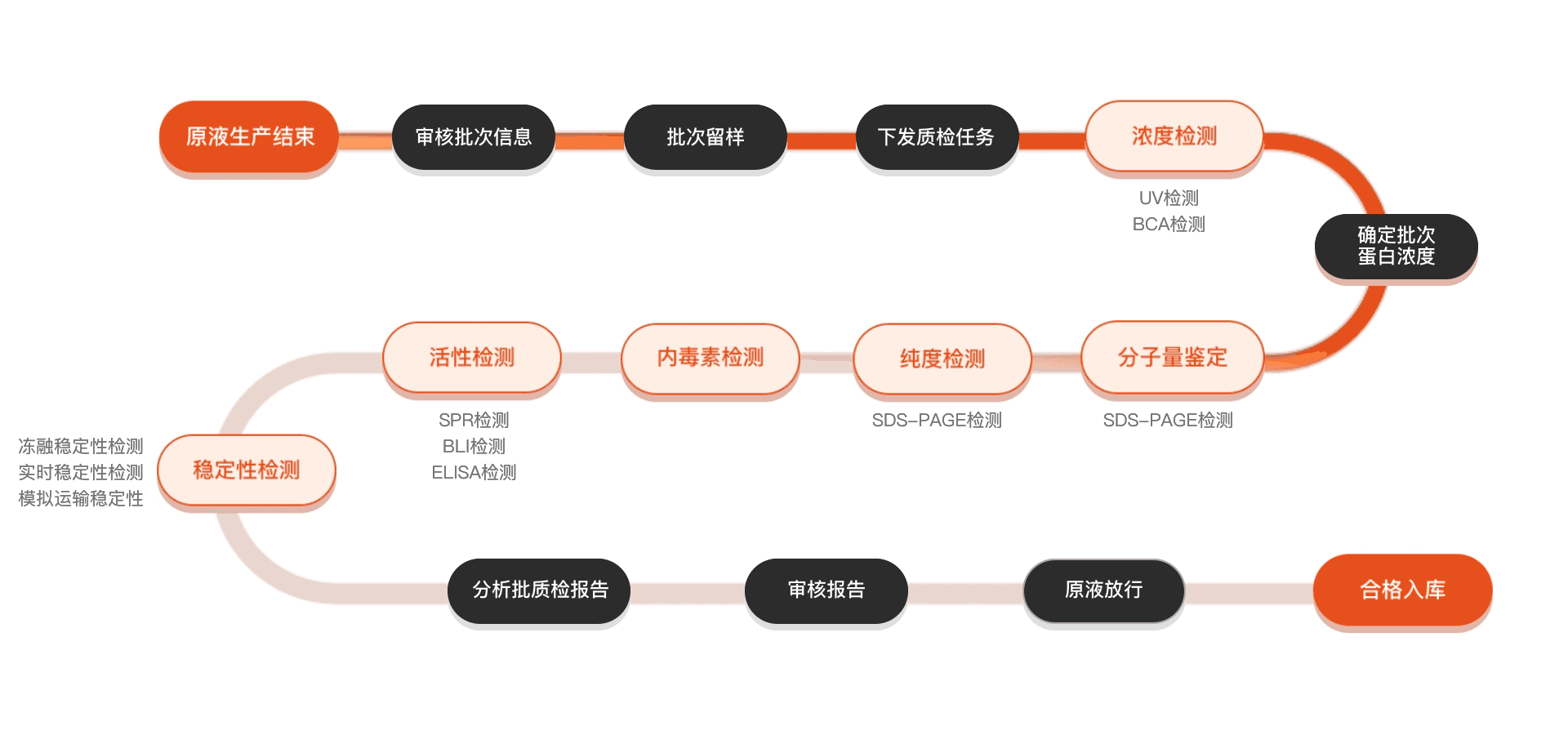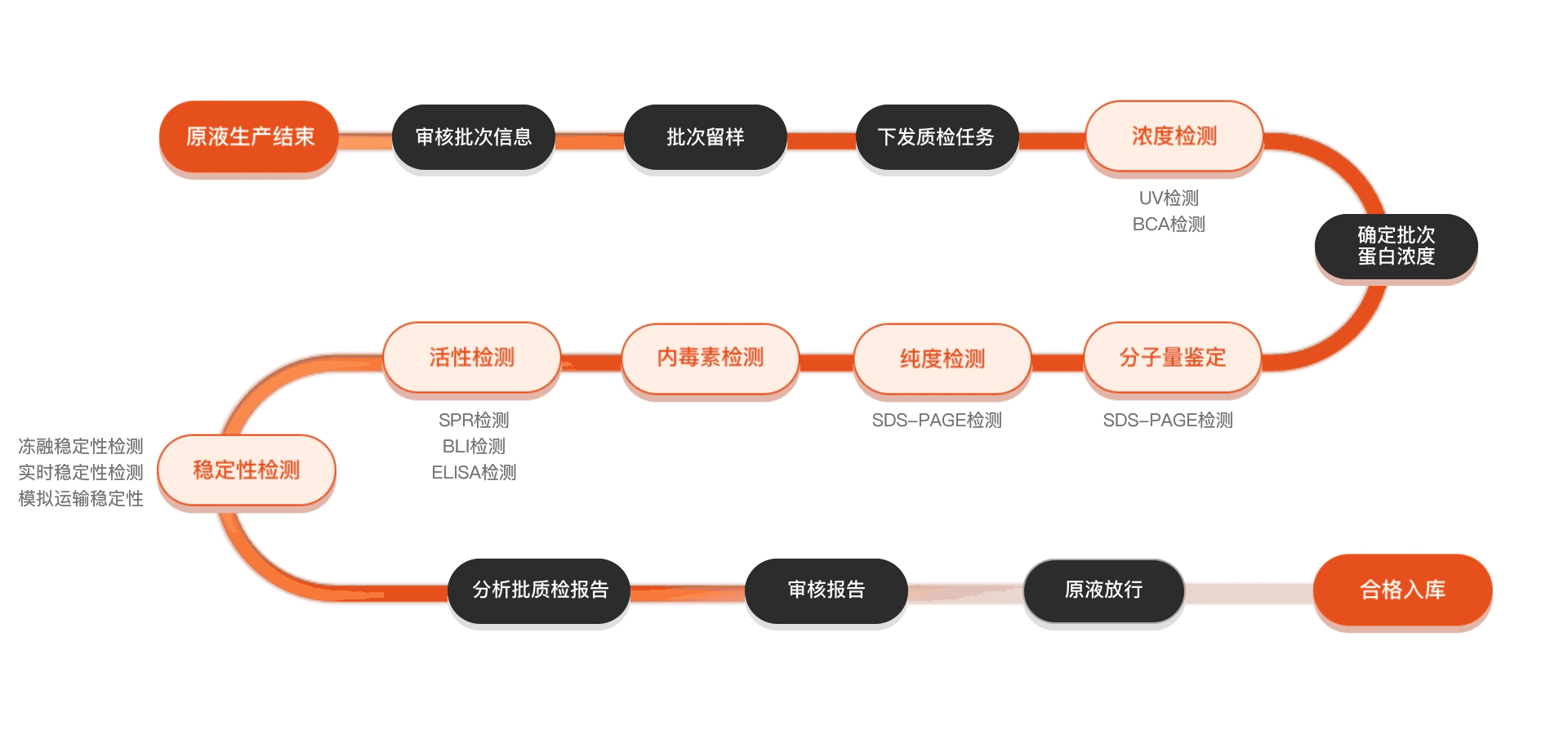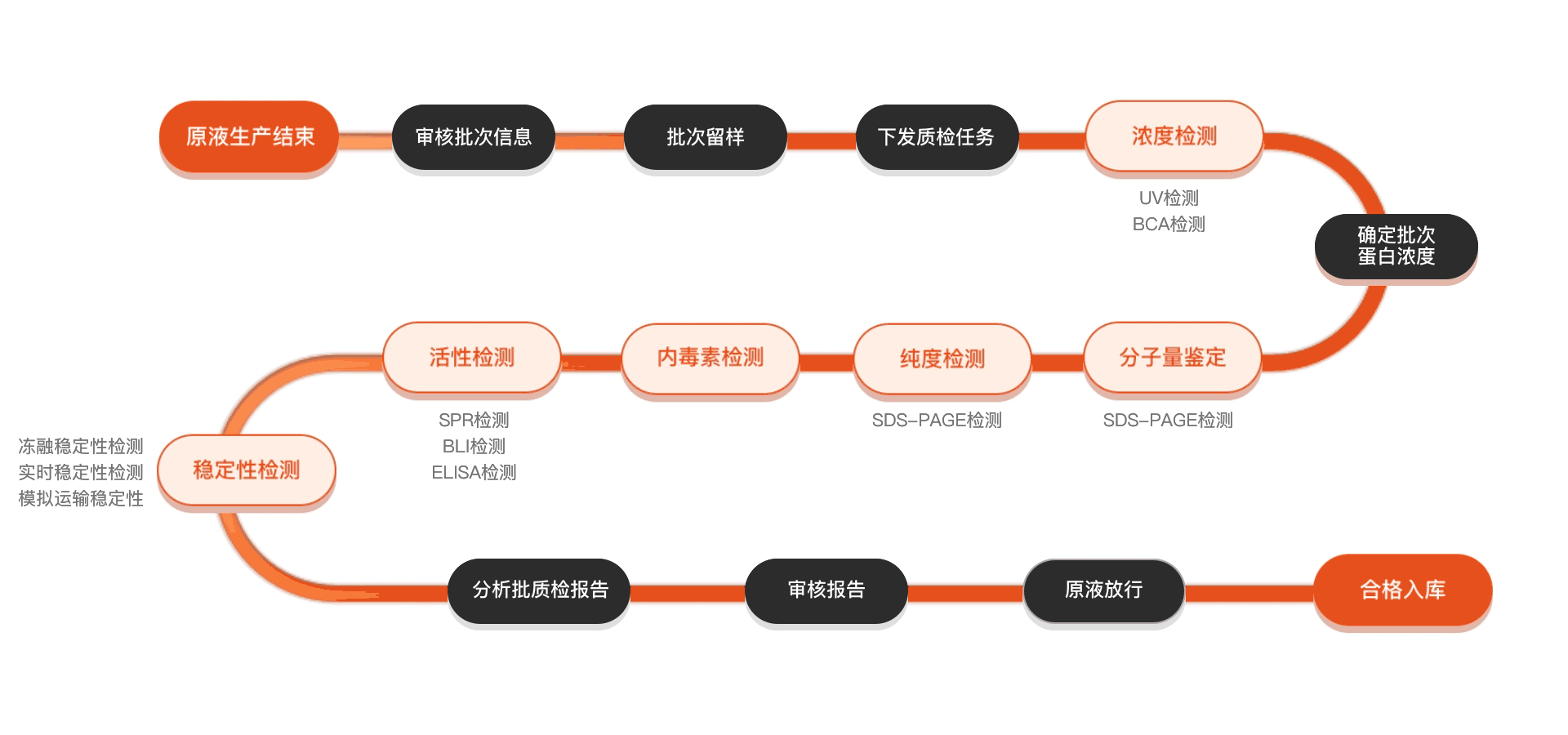
相关产品
背景信息
Fractalkine, also known as CX3CL1, is a unique chemokine that exists in both a soluble form and a membrane-bound form, allowing it to play a dual role in immune response and cell signaling. It primarily interacts with its receptor CX3CR1, which is expressed on various immune cells, including monocytes, T-cells, and microglia. The Fractalkine/CX3CL1 axis is crucial for regulating leukocyte adhesion and migration, particularly in inflammatory conditions. Research has demonstrated that this signaling pathway is involved in several pathophysiological processes, including neuroinflammation in neurological disorders, cardiovascular diseases, and cancer metastasis. Recombinant Fractalkine/CX3CL1 proteins are valuable tools in experimental studies aimed at understanding the molecular mechanisms underlying these diseases. By utilizing recombinant proteins, researchers can investigate how Fractalkine regulates immune cell behavior, the role of the CX3CR1 receptor in immune system modulation, and the therapeutic potential of targeting this pathway. The development of recombinant Fractalkine/CX3CL1 not only facilitates basic research but also contributes to the exploration of potential therapeutic strategies for diseases characterized by aberrant inflammation and immune responses. Consequently, studies involving recombinant Fractalkine are critical for elucidating its biological functions and implications in health and disease, paving the way for future clinical applications.